能垒(EB | Energy Barrier)计算
计算样例
1) 电催化能垒
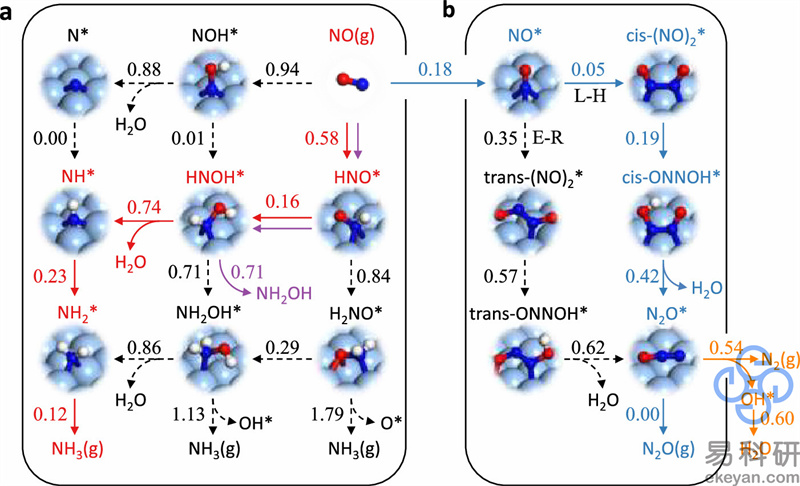 J. Phys. Chem. Lett. 2021, 12, 29, 6988–6995
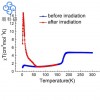
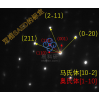
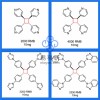
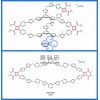
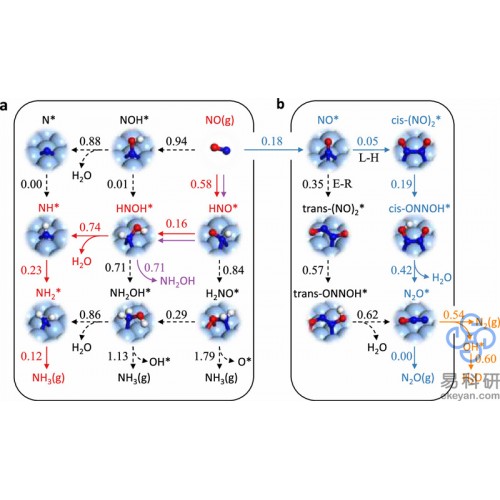
中科院大连化物所肖建平团队利用Ag电极作为模型催化剂,结合第一性原理计算与微观动力学模拟,首先验证了电催化能垒计算中采用单层水模型的可靠性;随后,考虑完整的NO还原反应网络,计算得到其所有的能量信息;最后建立了微动力学模型。研究发现,计算得到的产物选择性随外加电势的变化趋势与实验结果一致:随着电势降低,NO-NO的热化学耦合反应受到抑制而氨气的选择性升高;进一步降低电压,电催化析氢反应(HER)就会占主导作用,这是由于HER的电荷转移系数越大,受电势的影响越强。该模型还有助于理解其他电催化还原反应的电势依赖性,为实现电催化NOx转化的选择性控制提供了理论基础。
J. Phys. Chem. Lett. 2021, 12, 29, 6988–6995
中科院大连化物所肖建平团队利用Ag电极作为模型催化剂,结合第一性原理计算与微观动力学模拟,首先验证了电催化能垒计算中采用单层水模型的可靠性;随后,考虑完整的NO还原反应网络,计算得到其所有的能量信息;最后建立了微动力学模型。研究发现,计算得到的产物选择性随外加电势的变化趋势与实验结果一致:随着电势降低,NO-NO的热化学耦合反应受到抑制而氨气的选择性升高;进一步降低电压,电催化析氢反应(HER)就会占主导作用,这是由于HER的电荷转移系数越大,受电势的影响越强。该模型还有助于理解其他电催化还原反应的电势依赖性,为实现电催化NOx转化的选择性控制提供了理论基础。
收费标准
根据计算具体需求评估计算工期和费用,详情请联系在线客服
能垒(EB | Energy Barrier)
在受动力学限制的化学反应中,活化能 Ea 为活化碰撞的平均摩尔能量与所有碰撞的平均摩尔能量之差;而能垒E为活化络合物与反应物的零点能之差。 能垒大则不易形成活化的中间产物,反应难以进行。能垒E为活化络合物与反应物的零点能之差,是不同于活化能的。一般的化学反应都是在等温等压下进行,自发跟非自发是看delta G也就是吉布斯自由能变。 无论哪种,要突破能垒,也就是活化能,都是因为要经历一个过渡态(transient, or say, transition state)。 自发跟非自发说的是热力学 (thermodynamics), 活化能高低说的是动力学(kinetics)。活化分子含有的能参加化学反应的最低限度的能量,称为化学反应的能垒,或称能阈或能障。